| ■βタンパクの切り出し |
それでは,アミロイド前駆体タンパクの遺伝子が異常になるとなぜアルツハイマー病になるかということですが,アミロイドの前駆体タンパク質というのは膜を一回貫通して存在しているタンパク質です(図10)。ここに細胞がありますと,核があって,これは細胞膜を例にとっていますけれども実際はこういうところにあるというよりも,細胞の中の膜に存在するわけですけども。例えばこういうところにあるとすると,このちょうど,膜を貫通する部分から外に出たこの辺ぐらいまで,この赤で塗ったところがβタンパクとして切り出されてくると,先程言った老人斑にたまっていたあのアミロイドというものになって線維状になって沈着します。正常ではなぜこういうのが出来ないかというと,これがみんなばらばらに分解されて処理されてしまう。つまりアミロイド前駆体タンパクというのはどうも必要なものらしい,それである機能が終わるとこれはばらばらにして分解してちょんぎって捨てられる。ところがアルツハイマーの人はここのところが切れない,あるいは特異的にここのところだけがどんどん切られて出てくる,その結果線維状になって溜ってしまう。これがアミロイド前駆体タンパク質からアミロイドが出来る機序です。
もう少し詳しくみてみましょう。いま膜を貫通して存在していて,その膜の貫通の途中部分から外に出た部分,ここに赤い部分があって,この部分が切り出されてくるとβタンパクと言われるタンパクになって,このタンパク質が非常に凝集しやすいものですから,凝集して沈着して老人斑にたまってしまう,ということです。このタンパク質は40個位のアミノ酸からなるタンパク質で,40と42とではとても意味が違います。たった2個のアミノ酸がここにくっついているだけなのですが,40というのは普通我々も結構作り出していて,ところが非常に溶けやすいもんですから,どんどん流れていって,どっかに出ていって処理される。ところが42個になってしまうとどうも凝集しやすくて脳にたまるようになります。42を切り出すそういうハサミ(酵素)がどうも悪いことをしているらしい,ということが最近になっていわれています。
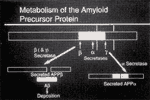
その切り出しのメカニズムはどうなっているのか,ということですが,又おなじアミロイド前駆体タンパク,先程赤で描いたところは白で描いてますが,正常では細胞の膜というのは脂質二重膜といって,外側の膜と内側の膜の2枚でできています。これを貫通して膜の途中部分から外に出たところ,ここからβタンパクができるのです。正常では,こういうハサミを使います。つまり,普通の人ではここにαと描いてあるところにハサミが入っているのです。その結果,βタンパクといわれている,この白い方の真ん中にハサミが来ています。そしてこの部分が細胞の外に放り出されて,何らかの働きをする。従って,まず真ん中でずばり切られてしまうとβタンパクというものはできないわけです。ところがアルツハイマー病の方はこのハサミの切れが鈍ってしまって,βとγというハサミをどんどん使います。その結果,こういう切り出しが起こり,そのためにβタンパクが沈着してしまうわけです(図12)。それなら,βとγのハサミとは一体なんだろう,これは酵素ですから,この酵素を早く見つければ,ということで世界中が血眼になって探しているのですが,いまだにまだわかりません。だけど,もしこの3つのハサミが判ったならば,αのハサミを促進してよく切れるようにしてやって,こっちの分解を早めて多くして,そしてγとβのハサミを鈍らせてやる。そうしたらアルツハイマー病の進行は押さえられる,あるいは予防できるのではないかということで世界中の製薬メーカーはこれの研究に束になってかかっている,というのが現状です。もう近々こういうものが見つかる,もう本当に数年以内に全部分かるはずです。そうすると予防薬,治療薬というのは先が見えてくる,というふうに期待できます。
アミロイド前駆体のタンパク質ですが,タンパク質というのはアミノ酸が並んでできたものです。これはアミノ酸の配列をかきましたけれども,膜の貫通部分がここからここまで,これら内側は膜の内側,これから外側,ということになります。今いいましたように膜の途中から,この辺からこうアミノ酸が,A,I,V,V,G,G,V,M,L,G,I,これはアミノ酸の略語です,グリシンとか,リジン,アスパラギンとか,セリン,バリン,こういうふうにアミノ酸の名前がずうっとありまして,ここがハサミで切れる,これがβのハサミ,ここで切れる,これがαのハサミ,ここで切れる,この辺で切れる,これがγの,ということになります。 それで,先程言いましたような,ああいう家系が見つかりました。その家系ではどういうことがおこっているかというと,例えばスエーデンで見つかった家系は,このβで切るハサミの直前のアミノ酸2個が突然変異で変わっています(図13)。Kというのはリジンですが,リジンがN,アスパラギンに変わって,Mというのはメチオニン,メチオニンがLというロイシンに,二つとも変わっています。こういうことが起こるとなぜか,非常に早くアルツハイマー病にかかるということがわかっています。それは恐らくこれが変わることによって,βのハサミが切れやすくなったのではないかというふうに推定されています。βが切れやすいとこのアミロイドがどんどん出てくるのではないかということです。
それからここに717番目,これはバリンというアミノ酸で,このバリンというアミノ酸が,イソロイシン,I,とか,F,フェニルアラニンとか,G,グリシン,こういうふうなアミノ酸に変異する家系が世界中で見つかりました。これは日本にも5家系くらいみつかりました。これも,ちょうどγのハサミのすぐ側にあります。このバリンがあることによってこのγのハサミがあんまり効かないようになっています。ところがそれが他のアミノ酸に変わることでγのハサミがどんどん切れだしていく。従ってβタンパクがどんどん切り出されてきて,老人斑にたまり,アルツハイマー病になるのではないか,という推定がなされています。だからこの変異をいれた遺伝子を動物で発現してこのメカニズムを探ろう,という動物実験が今なされています。その結果,今の遺伝子に人間が持っていたのと同じ変異を入れてその遺伝子を強制発現させたマウスをつくる,そういうマウスはわずか半年で脳に老人斑がいっぱいできています。今までマウスにアルツハイマーの変化をつくった人はいない,いくら長生きしてもマウスというのは3年生きるのが精一杯でそこまで生きても決して老人斑というのはみられなかった。ところが遺伝子をマウスに発現することによってこういった老人斑ができるようになった。つまり,少なくとも老人斑という病的変化を,それはマウスで再現できているというところまで来ている。ですからもうじきハサミがわかって,ハサミが分かればその薬をマウスで実験してどういうものが変わらなくなるかどうかということが検証される,ということになります。こういうのをトランスジェニック・マウスといいます。
|
|
 |


|
| 図10 |
APP膜貫通型タンパク質
|


|
| 図11 |
42個のアミノ酸からなるタンパク質は凝集しやすい
|

|
| 図12 |
アミロイド切り出しのメカニズム。
正常ではα部で切断。アルツハイマー病ではβとγで切断
|


|
| 図13 |
APPアミノ酸の配列
|
|